B
由每个特定AGO募集的一组其他效应物(图3)。在这里,我们
总结了目前的RISC目标识别和调控基因表达的机制的理解。
靶
mRNA
的识别
RISC中的小RNA在功能上分为4个结构域:种子区、中心区、补
充区和尾区(图2A)。种子区包括从引导链(g2-g8)的50端起
的第2至第8个核苷酸,其对于靶RNA的识别是关键的;中心区
(g9-g12)对于靶RNA和过客链的切割是重要的;补充区(g13-
g17)稳定靶结合;和尾区(g18-g17)稳定靶
3
0
e和
d
)如果对
数据集
进行
重新
定义
,
招募额外的因素,并决定RISC的命运RISC通过将包含g2-g5的
种子区的第一区段预组织成溶剂可接近的A型螺旋来发现靶标,
从而显著增加靶标结合的速率(Chandradoss等人,2015;
Salomon等人,2015)。g2-g5中的碱基配对触发人AGO 2中
HLA-7的移动,允许碱基对延伸至g8,其将30互补区(g13-
g17)重新定位为接近A-型(Schirle等,2014年)。由于引导链
的5
0
末端(g1位置)对接到AGO的5
0
结合口袋中,因此它不与靶
链的3
0
尽管如此,在t1(t1A)的腺嘌呤残基通过水介导的与由
L2接头和MID结构域形成的口袋的相互作用增加RISC在靶
mRNA上的停留时间
的AGO(Schirle等人, 2015)。
图3. miRNA相关RISC在动物
动物中的miRNAs通过多种机制沉默靶基因RISC通
过AGO中的色氨酸(W)结合口袋和GW 182中的
甘氨 酸-色氨 酸(GW)重复 之间 的相互作用 结合
GW 182
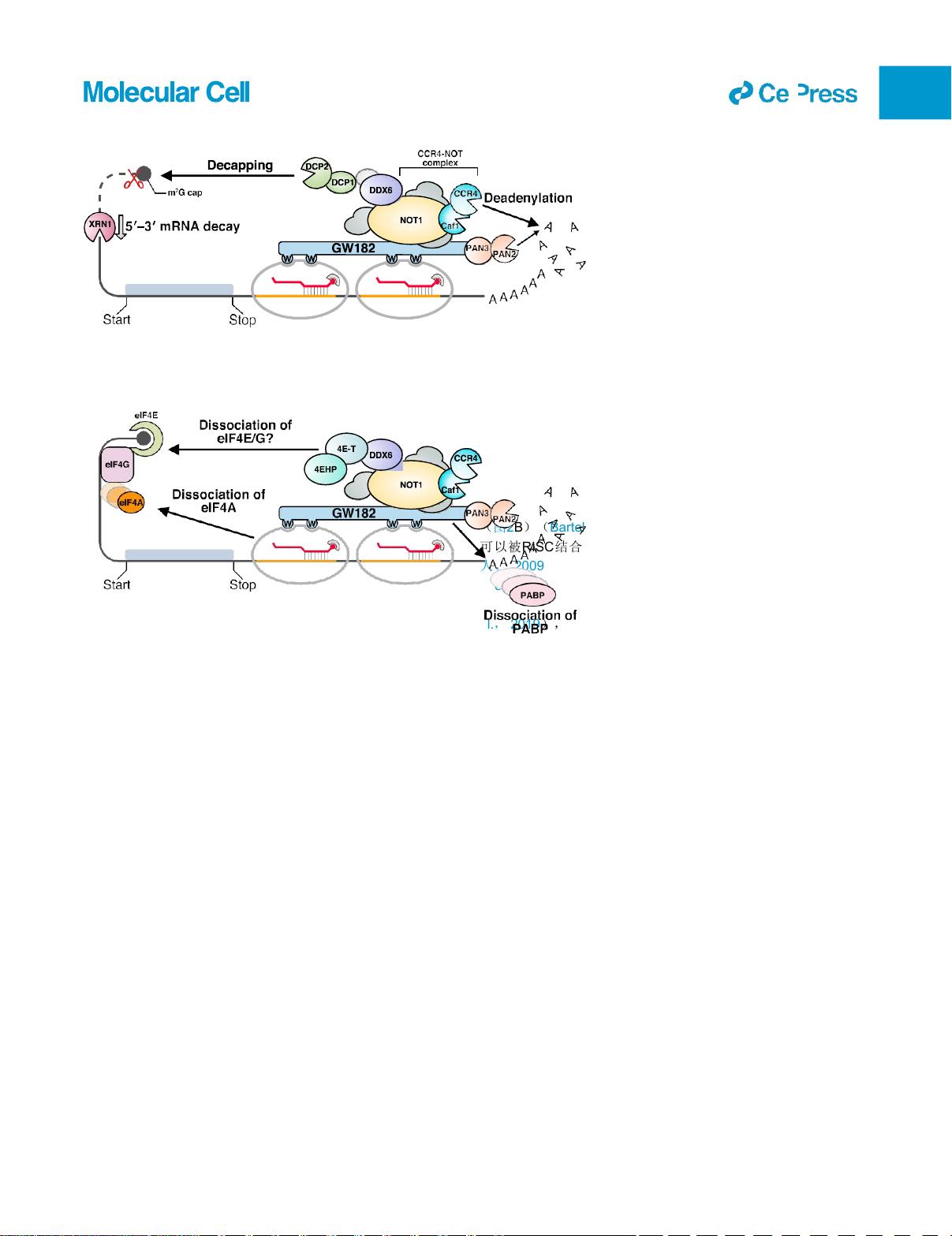
(A)
GW 182通过募集去腺苷化复合物CCR 4-NOT和
PAN 2-PAN 3以及去帽因子(包括去帽酶DCP 2)
来使靶mRNA不稳定。最后,XRN1以50到
30
的
方向
降解去帽mRNA。
(B)
动物RISC通过重组翻译抑制剂如DDX 6、4 E-T
和4 EHP抑制翻译起始,这些抑制剂被假设靶向eIF
4 E或eIF 4G。动物RISC还诱导PABP(一种翻译增
强子)从靶mRNA的poly(A)尾解离此外,RISC
可以 诱 导不 依 赖 于GW182的 起 始因子 eIF4A的 解
离。这些模型主要基于人类、苍蝇和蠕虫的生化研
究(Duchaine和Fabian,2019)。
哺乳动物RISC的最高亲和力靶标与g2-
g8以及在残基t1处的腺嘌呤具有完美的互
补性除了8-mer位点之外,与g2-g8(
(图2B)(Bartel,2018)。虽然种子中带有错配的非典型位点
可以被RISC结合,并且通常使用交联和其他方法检测(Chi等
人, 2009,2012; Hafner 等人 , 2010; Helwak 等人, 2013;
Loeb等人, 2012; Grosswendt等人,2014),它们具有低得多
的亲和力,并且需要沿着引导物更广泛的碱基配对(Beckeret
al., 2019),基本上不清楚细胞后果。
酵母和人RISC之间的结构相似性表明,上述动物miRNA靶识
别过程在真核RISC中基本上是保守的(Naka-nishi等人,2012;
Schirle和MacRae,2012; Elkayam等人,2012年)。然而,对
于稳定结合的引导链和靶RNA之间的互补性的要求在不同RISC
中显著不同。例如,中心区和尾区中的错配损害靶与
果蝇
Ago2
的结合,所述果蝇Ago2是抗病毒siRNA效应子(Wee et al.,
2012年)。植物AGO 1通常负载
50
U 21-nt miRNA和siRNA,也
需要 广泛 的碱 基配对以稳定结合和切割 靶RNA (Iwakawa 和
Tomari,2013)。单独的种子配对不足以稳定靶结合的事实可
能有利于确保这些RISC沉默的保真度。最近来自海绵Ephydatia
fluviatilis(Ef Piwi)的PIWI-进化枝AGO蛋白的冷冻电子显微镜
结构证明,与人AGO 2相比,Ef Piwi产生较弱的种子,并且需要
更长的配对用于靶结合(Anzelon et al.,2021年)。同样的机
制可能适用于那些需要