多模态单细胞追踪技术揭示肿瘤演进的精细进化树
72 浏览量
更新于2024-06-18
收藏 2.22MB PDF 举报
"肿瘤演变的多模态单细胞追踪技术揭示出详细的进化树"
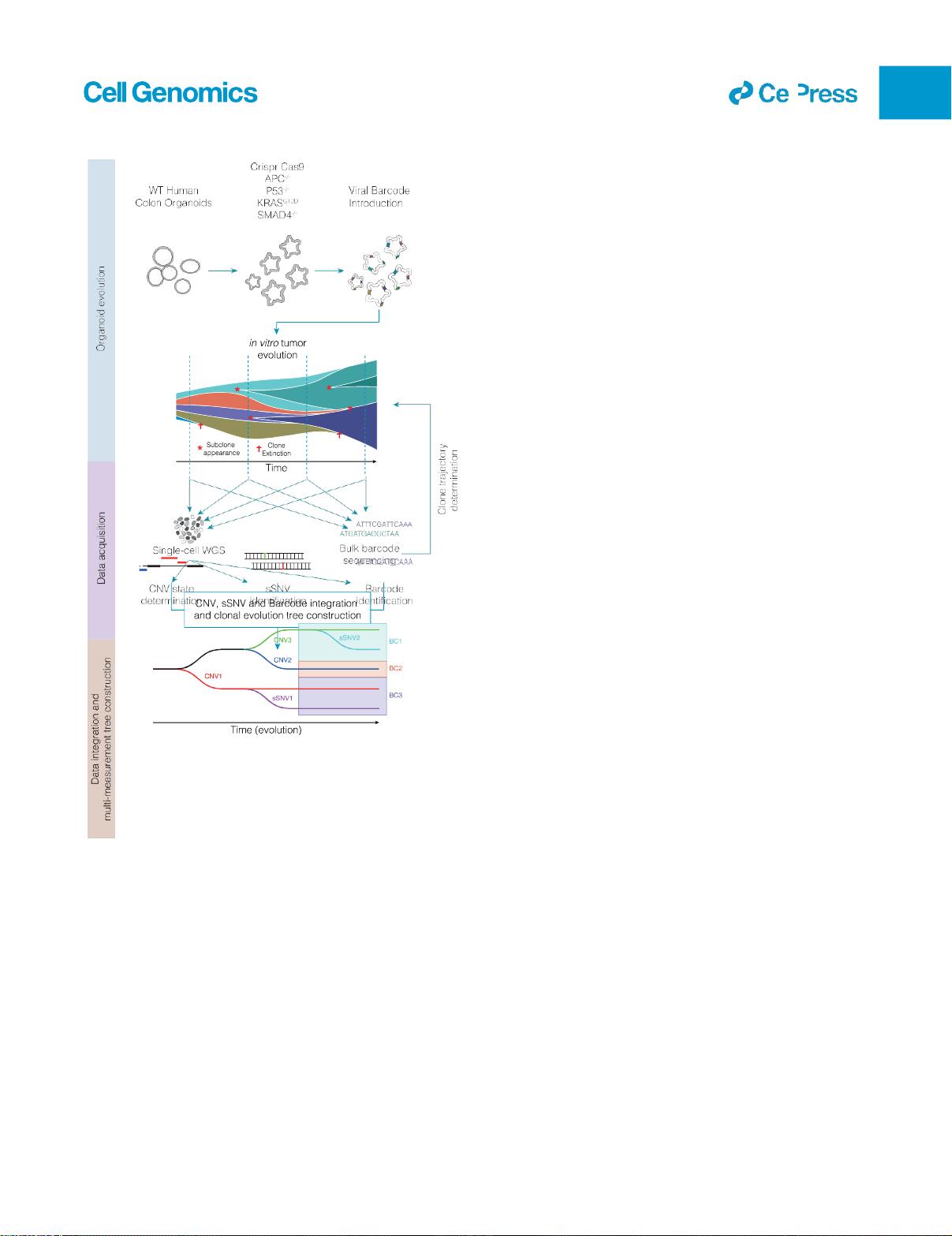
这篇文章深入探讨了一种创新的多模态单细胞追踪技术,用于研究肿瘤的演变过程。该技术结合了全基因组测序和谱系追踪,使得科学家能够以前所未有的细节水平解析肿瘤细胞的遗传变化和进化路径。通过这种方法,研究者们能够重建肿瘤的复杂进化树,揭示不同细胞群体之间的关系和演变历程。
在文章中,研究人员应用这项技术分析了结肠癌类器官,这是一种体外培养的肿瘤模型,可以模拟体内肿瘤的行为。他们发现,通过同时测量单细胞的拷贝数变异(CNV)、单核苷酸变异(SNV)以及病毒谱系条形码,可以构建出高度详细的进化树。这些数据揭示了肿瘤细胞在进化过程中经历的染色体丢失事件,例如染色体18和4的顺序丢失,这些丢失可能与肿瘤细胞的适应性优势有关。
这一发现对于理解肿瘤的异质性和耐药性形成机制具有重要意义。染色体的丢失可能导致基因的失调,进而影响肿瘤的生长、侵袭和治疗反应。通过对这些事件的精确追踪,研究者可能能够预测肿瘤对治疗的反应,并为个性化治疗策略提供依据。
文章作者Lennart Kester、Buysde Barbanson、Anna Lyubimova等人的工作展示了多模态单细胞分析在肿瘤研究领域的潜力。他们的研究不仅提供了关于结直肠癌的新见解,也为未来研究其他类型的癌症提供了有力工具和技术平台。
通过开放获取的方式发布,这篇2022年的文章《肿瘤演变的多模态单细胞追踪技术揭示出详细的进化树》鼓励了更广泛的科学社区参与讨论和进一步的研究,以期推动肿瘤生物学和精准医学的发展。通过这样的研究,我们可以期望在未来找到更有效的方法来对抗癌症,提高患者的生存率和生活质量。
2024-11-16 上传
2022-12-26 上传
2016-06-18 上传
2024-08-07 上传
2019-08-27 上传
2024-05-01 上传
cpongm
- 粉丝: 5
- 资源: 2万+
最新资源
- forward_algorithm.zip_matlab例程_matlab_
- solrium:Solr的通用R接口
- newunobet:大pp
- project_euler:这是来自https的已解决问题的存储库
- webchem:来自网络的化学信息
- cartified:一个非常基本的购物车实施
- 7Applied-multi-dimensional-fusion-.zip_图形图像处理_PDF_
- risitas-uikit
- homework4-february-20-2021:Web API:代码测验
- astrofox:Astrofox是一种运动图形程序,可让您将音频转换为出色的视频
- SpotipyProject
- tdd-blog:只是学习TDD的一个示例
- ezknitr:使用“ knitr”时避免典型的工作目录痛苦
- webPass-crx插件
- vue+node少儿编程项目.zip
- test-workflow